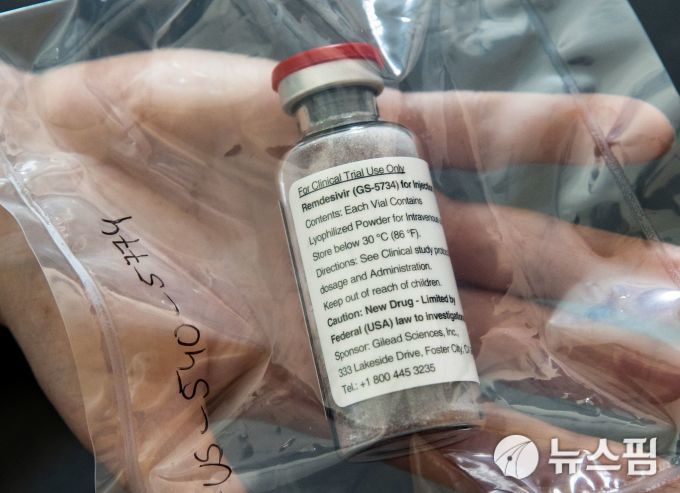
[서울=뉴스핌] 최원진 기자 = 미국 의사들과 보건 과학계는 당국이 코로나19(COVID-19) 중증 환자들을 대상으로 긴급 사용을 허가한 길리어드사이언스 사의 항바이러스제 렘데시비르의 임상 자료를 공개할 것을 요구했다고 로이터통신이 21일(현지시간) 보도했다.
미 제약기업 반다 파마슈티컬스의 마하엘 폴리메로풀로스 최고경영자는 이날 미 식품의약국(FDA)의 렘데시비르 긴급 사용 허가를 이끌어낸 모든 실험 결과와 자료를 제공할 것을 요구하는 내용의 공개서한을 발표했다.
그는 로이터에 "만약 이 약이 감염주기 초기 환자들에게 가장 잘 맞는다면? 우리가 그동안 자연스런 동점심으로 중증 환자들에게만 이 약을 제공했다면 우리는 약을 낭비했을지도 모른다"고 말했다.
FDA는 지난 1일 코로나19 중증 환자들을 대상으로 렘데시비르 긴급 사용을 허가했다. 이는 국립알레르기 및 감염병연구소(NIAID) 시험의 예비 결과를 토대로 내려진 결정이다. 플라시보 통제 실험 결과 렘데시비르 처방 환자 실험군의 평균 입원 기간은 플라시보 대조군 보다 31%, 약 4일 정도 줄었다.
실험은 코로나19 환자 1063명을 대상으로 진행됐으며 이밖에 다른 구체적인 실험 결과 내용은 공개되지 않았다. NIAID는 실험 보고서가 수 주 후에 발간될 것이라고 알렸다. 길리어드 측은 언제 이 보고서가 나올지 밝히지 않았다.
터프츠 의료 센터의 감염병 전문가 헬렌 바우처 박사는 "우리는 이 약으로 가장 효과를 보고 부작용 가능성이 낮은 환자들에게 제공하고 싶다"고 말했다.
한편, 병원들은 한정된 렘데시비르 약품의 불안정한 유통이 우려된다며 약품 사용에 대한 윤리적 가이드라인을 수립하고 있다.
휴스턴 감리교 병원의 감염병 의약전문가 캐서린 페레즈는 약물 실험 내용을 바탕으로 처방하고 있지만 더 나은 정보에 입각한 치료 결정을 내리기 위해서는 더 많은 데이터가 필요하다고 했다.
NIAID는 항염증 화합물과 결합한 렘데시비르 치료 효과를 연구할 계획이다.
wonjc6@newspim.com
 영상
영상